Ghidul Tău HER Genes
Ai multe întrebări? E firesc. HER Genes e locul în care găsești răspunsuri clare, sprijin și informații pe înțelesul tău — fără presiune, fără grabă.
HBOC - Perspectiva geneticianului

Dr. Maria Miclaus, Medic Specialist Genetica Medicala si Endocrinologie
1) Ce este HBOC?
HBOC (Hereditary Breast and Ovarian Cancer) este un sindrom genetic în care riscul de a dezvolta cancer de sân și/sau cancer ovarian este mult mai mare decât în populația generală, din cauza unor mutații moștenite.
- Apare de obicei în familii unde mai multe rude au avut cancer de sân/ovar, adesea la vârste tinere.
- Se transmite autozomal dominant — dacă unul dintre părinți are mutația, există 50% șanse să fie moștenită de către fiecare copil.
Gene cu risc înalt
Gene cu risc moderat
Gene cu risc mic
diverse polimorfisme (SNPs)
2) Când investigăm riscul de HBOC?
Dacă în familie există cazuri de cancer de sân sau ovarian, mai ales la vârste tinere, riscul de sindrom HBOC trebuie investigat.
Criterii frecvente pentru testare genetică HBOC:
- Cancer de sân diagnosticat la vârste <50 ani
- Cancer ovarian la orice vârstă
- Cancer de sân triplu negativ
- Cancer de sân multicentric
- Cancer de sân la bărbat
- Mai multe rude apropiate cu cancer de sân/ovar/prostată/pancreas
Sindromul HBOC văzut prin ochii unui ginecolog

Dr. Georgiana Nemeti, Medic Specialist Obstetrică-Ginecologie
Pe scurt – ce ar trebui să reții
- HBOC este un sindrom ereditar care crește riscul pentru cancer de sân și de ovar; nu toate cazurile sunt ereditare.
- Genele implicate (ex. BRCA1/2, RAD51C/D, BRIP1, PALB2; MMR în sindromul Lynch) au rol în repararea ADN‑ului.
- rrBSO (îndepărtarea trompelor și ovarelor) scade important riscul de cancer ovarian; există totuși un risc rezidual peritoneal.
- Leziunile STIC sunt forme incipiente depistate microscopic și confirmă utilitatea intervenției profilactice.
- Păstrarea fertilității este posibilă (ovocite/embrioni/țesut ovarian, PGT‑M) și trebuie discutată înaintea intervenției.
Dr. Georgiana Nemeti – medic specialist obstetrică-ginecologie
Cum începem – ascultând povestea
De fiecare dată când o femeie intră în cabinetul meu și îmi spune că are o mutație genetică sau un istoric familial de cancer, respirăm împreună. Nu doar pentru a domoli teama, ci pentru a da sens acelei informații. În spatele unui rezultat genetic există o poveste, un arbore genealogic al emoțiilor, al pierderilor și al speranțelor.
Ce este sindromul HBOC?
HBOC (Hereditary Breast and Ovarian Cancer) este o afecțiune genetică moștenită care crește riscul de a dezvolta cancer de sân, de ovar și, uneori, și alte tipuri de cancer (ex. endometru, pancreas, colon, stomac). Majoritatea pacientelor cu cancer de sân sau ovar au forme sporadice; doar un procent mic au forme moștenite.
În HBOC sunt implicate gene ce participă la repararea ADN-ului. Când ele au variante patogene, repararea devine ineficientă și cresc șansele apariției unui cancer.
Cât de frecvent este?
- Aprox. 1 din 10 cancere de sân este ereditar și aprox. 20 din 100 de cancere de ovar sunt ereditare
- În populația generală, 1 din 300 de femei poartă o mutație patogenă (cel mai adesea BRCA1/2).
- Riscul de-a lungul vieții de a face cancer ovarian este sub 2% în populația generală, dar poate urca mult pentru purtătoarele de mutații patogene
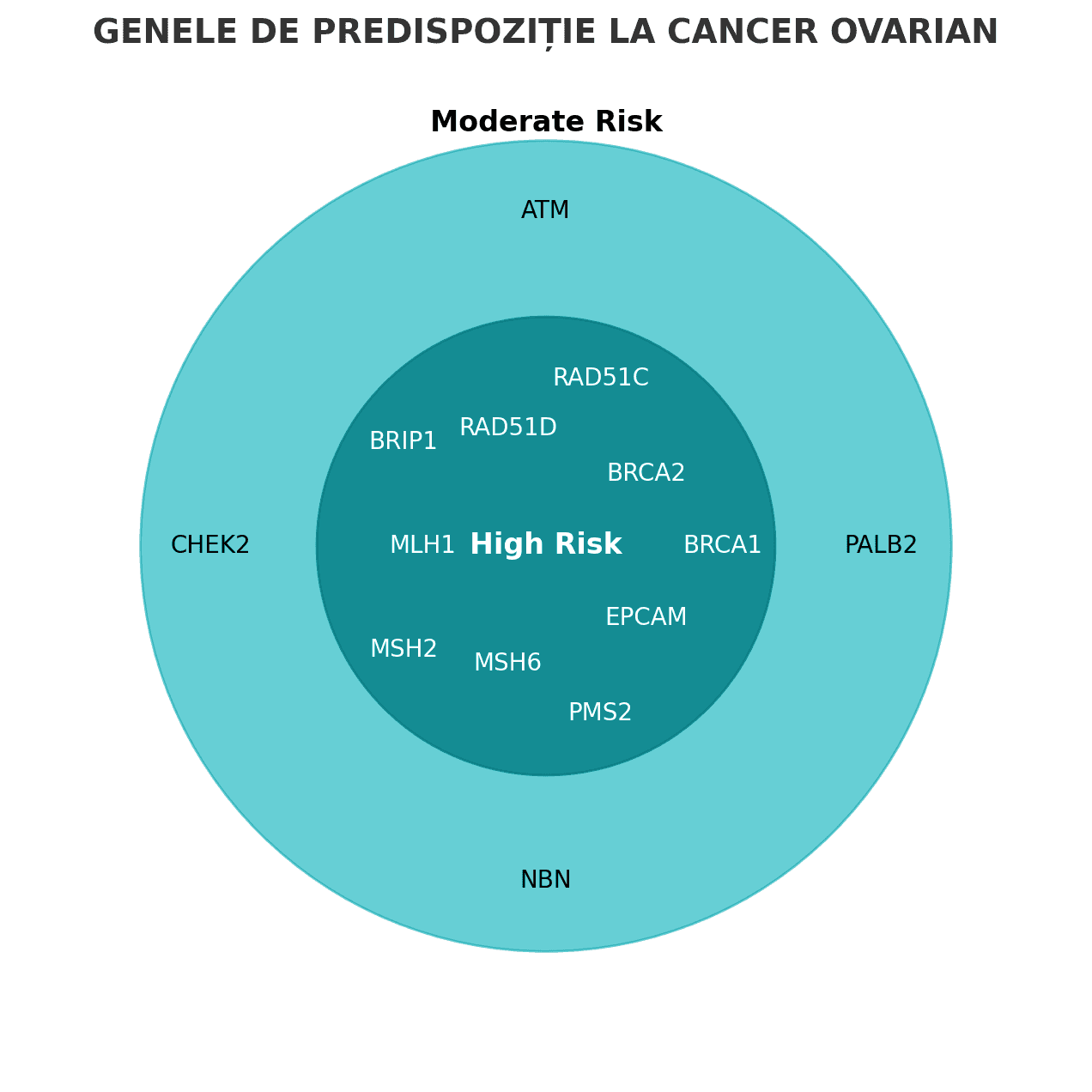
Ce gene sunt implicate în riscul de cancer ovarian?
Iată câteva dintre genele mai frecvent implicate în cancerele ginecologice: BRCA1, BRCA2, RAD51C, RAD51D, BRIP1, PALB2; gene MMR (MLH1, MSH2, MSH6, PMS2) în sindromul Lynch. Toate sunt implicate în repararea ADN-ului (recombinare omoloagă/RAD sau repararea nepotrivirilor – MMR).

Ce este rrBSO și de ce se recomandă?
rrBSO = risk-reducing bilateral salpingo-oophorectomy: îndepărtarea chirurgicală a ovarelor și trompelor uterine pentru a reduce semnificativ riscul de cancer ovarian (un cancer care, frecvent, este depistat tardiv).
Important: Chiar și după rrBSO, poate exista un risc rezidual de carcinom peritoneal primar, mai ales dacă se găsesc leziuni STIC la examenul histopatologic.
Ce sunt leziunile STIC și de ce sunt importante
Poate ai auzit că unele femei, atunci când aleg să facă o intervenție chirurgicală de reducere a riscului — adică îndepărtarea trompelor și ovarelor — primesc la finalul rezultatului anatomo-patologic o mențiune care sună îngrijorător: „leziune STIC".
STIC vine de la Serous Tubal Intraepithelial Carcinoma — adică o formă incipientă, microscopică de transformare malignă, descoperită de obicei în porțiunea finală a trompei uterine (numită fimbrie).
Această leziune nu este încă un cancer invaziv, ci o celulă aflată la începutul drumului către cancer, un semn că procesul de transformare a început în trompe, nu în ovare – așa cum mult timp s-a crezut.
De ce contează:
- Leziunile STIC sunt considerate prima etapă a cancerului seros de ovar — cel mai frecvent și agresiv tip.
- Ele pot fi depistate doar la microscop, printr-o analiză detaliată a trompelor, realizată după o intervenție profilactică.
- Prezența unei leziuni STIC confirmă că decizia chirurgicală a fost luată la timp și, de multe ori, a prevenit dezvoltarea unui cancer invaziv.
Ce trebuie să reții:
Dacă rezultatul tău arată o leziune STIC, nu este un diagnostic de cancer, ci o dovadă că ai acționat la timp. Totuși, pentru că aceste leziuni pot indica o predispoziție către apariția unor cancere seroase în alte zone (cum ar fi peritoneul), se recomandă o urmărire atentă în continuare — cu controale periodice și monitorizare imagistică.
Ce se discută la consilierea preoperatorie
- Riscul tău individual și cât scade el după rrBSO.
- Alternativele (mai puțin eficiente): salpingectomie profilactică; supraveghere la 6 luni cu ecografie + CA125; contraceptive orale.
- Consecințe: infertilitate și menopauză prematură (uscăciune vaginală, scăderea libidoului, tulburări de somn, bufeuri, osteoporoză, schimbări de dispoziție, risc coronarian).
- Riscul de a găsi un cancer ocult: probabilitate raportată în literatură 0,6–18,5%; e necesar consimțământ pentru o posibilă intervenție suplimentară în timpul operației.
- Prezervarea fertilității
Cum îți poți păstra fertilitatea – speranță și știință în același timp
Pentru multe femei tinere, aflarea că poartă o mutație patogenă BRCA sau decizia de a face o salpingo-ooforectomie profilactică (rrBSO) vine cu o întrebare firească și dureroasă:
„Voi mai putea avea copii?"
Este o întrebare legitimă, și trebuie discutată deschis, încă de la primele consultații. Vestea bună este că medicina actuală oferă mai multe soluții reale de prezervare a fertilității, care pot fi adaptate fiecărei paciente, în funcție de vârstă, dorința de maternitate și momentul planificat al intervenției.
Înainte de orice decizie, recomandăm evaluarea rezervei ovariene — prin dozarea hormonului AMH și ecografie transvaginală pentru numărarea foliculilor antrali. Acest pas ne ajută să estimăm potențialul reproductiv și să alegem cea mai bună strategie.
Iată opțiunile principale, așa cum le folosim în practica clinică și cum le recunoaște literatura de specialitate:
1. Crioprezervarea ovocitelor (ovulelor)
Este cea mai utilizată metodă de prezervare a fertilității la femeile tinere. Se realizează printr-o stimulare ovariană controlată, urmată de puncție foliculară și recoltare a ovocitelor mature, care sunt apoi congelate prin vitrificare. Procedura durează în general 10–12 zile și nu întârzie semnificativ programarea unei intervenții chirurgicale profilactice. Este ideală pentru femeile care nu au încă un partener sau care doresc să amâne sarcina. Rata de succes depinde de vârstă, dar rezultatele moderne arată șanse bune de obținere a unei sarcini după dezghețarea și fertilizarea ovocitelor.
2. Crioprezervarea embrionilor
Este o metodă potrivită pentru cuplurile stabile. După stimularea ovariană, ovocitele sunt fertilizate in vitro cu sperma partenerului, iar embrionii rezultați sunt congelați pentru o utilizare ulterioară. Această metodă are cele mai ridicate rate de succes în obținerea unei sarcini, dar necesită consimțământul ambilor parteneri și planificare atentă.
3. Crioprezervarea țesutului ovarian
Aceasta este o opțiune valoroasă pentru femeile foarte tinere sau pentru cele care nu pot amâna intervenția chirurgicală. Țesutul ovarian este recoltat laparoscopic, apoi crioprezervat în fragmente mici și, ulterior, poate fi reimplantat pentru a restabili funcția hormonală și, uneori, chiar fertilitatea naturală. Este o metodă tot mai utilizată în centrele mari, mai ales la femeile care nu pot beneficia de stimulare hormonală.
4. Fertilizarea in vitro cu diagnostic genetic preimplantațional (PGT-M)
Pentru cuplurile care doresc să evite transmiterea mutației genetice viitorilor copii, există posibilitatea PGT-M, o analiză care identifică embrionii fără mutația respectivă înainte de implantare. Astfel, femeia poate duce o sarcină sănătoasă fără riscul de a transmite mutația. Această decizie este complexă, necesită consiliere genetică aprofundată și sprijin emoțional, dar oferă o șansă reală la o maternitate fără teamă.
Alte opțiuni și considerente
- În unele cazuri, pacienta poate opta pentru preservarea fertilității concomitent cu intervenția chirurgicală profilactică, dacă există o echipă multidisciplinară experimentată.
- Specialistul în medicina reproductivă are un rol esențial în consilierea deciziei și evaluarea riscurilor.
- În paralel, pacientele pot fi informate despre opțiunile de adopție, donare de ovocite sau alte metode de maternitate asistată, dacă acestea sunt în acord cu dorințele și valorile personale.
Menopauza chirurgicală & bunăstare
După rrBSO, menopauza apare brusc și simptomele pot fi mai intense decât în menopauza naturală. Management posibil:
- terapie de substituție hormonală (unde este sigură medical),
- suport pentru sănătatea osoasă, mișcare, alimentație și hidratare,
- consiliere psihologică și sexuală.
Informații utile despre sindromul Lynch din prisma medicului ginecolog
Sindromul Lynch (neoplasm colorectal ereditar non-polipozic) crește riscul pentru cancer de endometru, ovare, colon și alte localizări. Femeile trebuie să ceară asistență medicală promptă la orice sângerare uterină anormală.
Reducerea riscului: pentru prevenirea cancerului de endometru și ovar, se recomandă histerectomia totală cu salpingo-ooforectomie bilaterală (THBSO), de regulă între 35–45 ani, după împlinirea potențialului fertil. Se recomandă consiliere timpurie cu specialist în medicina reproductivă (inclusiv PGT/diagnostic prenatal, opțiuni de fertilitate).

Sdr Lynch – importanța monitorizării până la intervenția chirurgicală profilactică
- Prelevare anuală de probe endometriale (începând cu 30–35 ani sau cu 5–10 ani înaintea celei mai timpurii vârste din familie la care a apărut un cancer de endometru).
- Ecografie transvaginală anuală sau biopsie endometrială anual/bienal (conform ESGO/ESTRO/ESP).
- Recomandări NCCN & ACOG: biopsie la fiecare 1–2 ani, începând cu 30–35 ani.
- Dacă se operează pentru cancer colorectal: se poate lua în calcul THBSO concomitent (individualizat).
Posibilități de screening pentru cancerul ovarian la femei purtătoare de mutații patogene BRCA și BRCA-like
Deși implicarea genelor este clară, nu există metode eficiente de screening pentru cancerul ovarian. Până acum, nu există dovezi că supravegherea periodică (ex. ecografie + CA125 la 6 luni) reduce mortalitatea în aceste grupuri cu risc înalt.
Alte gene implicate în cancere ginecologice & situații speciale
- BRIP1, RAD51C, RAD51D (risc 5–20%) și PALB2 (3–5%): decizia privind rrBSO se personalizează, de regulă în jurul vârstei de 45–50 ani.
- Dacă ai o testare genetică neconcludentă însă un istoric familial puternic, poți fi candidată la rrBSO după evaluarea atentă a beneficiilor și riscurilor.
De reținut
Nu toate femeile cu istoric familial au o mutație; nu toate mutațiile duc sigur la cancer. Consilierea și testarea genetică te ajută să iei decizii informate. Profilaxia chirurgicală – adică îndepărtarea ovarelor, trompelor și uneori și a uterului (rrBSO/THBSO) se indică, în majoritatea situațiilor, după îndeplinirea potențialului fertil și poate salva vieți. Întârzierea intervenției poate crește riscul de leziuni premaligne sau maligne oculte identificate intraoperator.
Dincolo de gene – despre încredere, alegere și viață
A ști că porți o mutație genetică nu este o condamnare, ci o chemare la grijă. E o șansă de a-ți rescrie povestea, de a lua decizii conștiente și de a trăi cu sens. Nu toate femeile aleg aceeași cale. Unele decid să intervină chirurgical devreme, altele preferă monitorizarea atentă. Unele se concentrează pe maternitate, altele pe stabilitate și echilibru. Indiferent de alegere, fiecare pas merită respect, sprijin și înțelegere. Medicina modernă nu mai înseamnă doar tratament – înseamnă prevenție, educație și empatie. Pentru mine, ca medic ginecolog, cel mai important lucru este să le reamintesc femeilor că nu sunt singure. Există soluții, există comunități, există viață dincolo de gene.
Întrebări pentru medicul tău
- Sunt eligibilă pentru rrBSO acum sau e mai bine să o programez după un anumit prag de vârstă?
- Ce opțiuni am pentru prezervarea fertilității și care mi se potrivește (ovocite, embrioni, țesut ovarian, PGT‑M)?
- Este sigură pentru mine terapia de substituție hormonală după rrBSO?
- Există semne/analize utile între timp, având în vedere că screeningul pentru cancerul ovarian nu reduce mortalitatea?
- Ce plan de urmărire recomandați după intervenție (controale, imagistică, analize)?
Conținut educațional HerGenes. Nu înlocuiește consultul medical. Pentru decizii personalizate, discută cu medicul genetician, ginecologul oncolog și senologul tău.
Perspectiva oncologului în sindromul HBOC — de ce contează să știi că porți o mutație BRCA

Dr. Ema Rohozăneanu, Medic Specialist Oncolog
Pe scurt – ce ar trebui să reții
- Informația că ești purtătoare BRCA poate deschide opțiuni de tratament țintit (ex. inhibitori PARP).
- Uneori, chimioterapia cu “platină” este preferată pentru sensibilitatea crescută a celulelor canceroase.
- În boala avansată, terapiile țintite pot îmbunătăți controlul bolii și calitatea vieții.
- Eligibilitatea se decide individual, în funcție de stadiu și riscul de recidivă.
Ce înseamnă că ai descoperit că ești purtătoare de mutație BRCA1 — și de ce contează
Ai aflat că ai cancer de sân (în cazul tău, triplu negativ) și că ai mutația BRCA1. Este un șoc, știu. Vreau să îți spun ceva esențial: acum avem un avantaj — nu pentru că ai mutația, ci pentru că aceasta ne spune informații importante despre “slăbiciunile” celulelor tumorale, pe care le putem exploata cu tratamente specializate.
Gândește-te așa: celulele canceroase care au mutații BRCA1 sau BRCA2 (sau alte defecte de reparare a ADN-ului) au o slăbiciune intrinsecă — nu pot repara eficient anumite daune la ADN. Iar asta poate fi folosit ca țintă de tratament.
Mai jos explic, pas cu pas, ce înseamnă asta pentru tine — ce opțiuni în plus poți avea, ce schimbă, ce trebuie să știi.
Cum ajută faptul că știm că ai mutația — ce opțiuni în plus apar
1. Tratament “suplimentar” după intervenția standard (adjuvant) — inhibitor PARP
După ce ai făcut intervenția chirurgicală, chimioterapie și, dacă e nevoie, radioterapie, există o opțiune pentru paciente cu mutație BRCA1 sau BRCA2: inhibitorii PARP (un tip de terapie țintită).
Un studiu mare numit OlympiA a arătat că la paciente cu mutație BRCA și cu cancer de sân HER2-negative (inclusiv triplu negativ) cu risc relativ ridicat de recurență, administrarea de olaparib pentru un an, după tratamentele de bază, reduce riscul ca boala să revină și îmbunătățește supraviețuirea.
Pe baza acestui studiu, ghidurile de oncologie (de exemplu cele ale ASCO) recomandă olaparib ca opțiune adjuvantă la paciente cu mutație BRCA1/2 și risc ridicat.
Deci, dacă ești purtătoare a unei variante patogene BRCA, se activează o opțiune care nu se aplică la toate pacientele și care poate oferi beneficiu suplimentar.
2. Alegerea chimioterapiei — sensibilitate la medicamente pe bază de platină
Celulele canceroase care au defecte în repararea ADN-ului (așa cum se întâmplă când există o mutație BRCA) sunt adesea mai sensibile la tratamente care rup sau distrug ADN-ul — cum sunt agenții pe bază de platină (cisplatin, carboplatin).
Prin urmare, oncologul poate decide să includă sau să prioritizeze în regimul tău un astfel de medicament, știind că ai mai multe șanse să răspunzi bine.
Acest lucru înseamnă că nu se merge “generic”, ci se rafinează chimioterapia într-o variantă care exploatează vulnerabilitatea celulelor tumorale.
3. Tratament în caz de boală avansată / metastatică
Dacă boala înaintează sau reapare (metastază), faptul că ai mutația BRCA îți oferă acces la terapii țintite cu inhibitor PARP (olaparib, talazoparib) — în loc să mergem doar pe chimioterapie obișnuită.
De exemplu, ghidurile ESMO recomandă ca paciente cu mutație germinală BRCA și cancer de sân metastatic HER2-negativ să fie tratate cu PARP în locul unora dintre chimioterapiile convenționale, pentru că astfel rezultatele pot fi mai bune și calitatea vieții mai bună.
Deci, în stadiile mai avansate, nu ești “la mâna întâmplării” — avem terapii țintite care pot fi mai eficiente pentru tine decât opțiunile standard.
4. Terapia de întreținere (în cancer ovarian, analog în alte contexte)
Deși cazul tău este sânul, este util să comparăm cu ce știm din cancerul ovarian, deoarece există o experiență mai multă acolo: după ce o tumoră ovariană răspunde la chimioterapie pe bază de platină, în cazul în care pacienta are mutație BRCA sau deficit de reparare a ADN (HRD), se poate administra un inhibitor PARP ca terapie de întreținere, pentru a prelungi perioada fără boală.
Aceasta demonstrează principiul: celulele canceroase care nu pot repara ADN-ul bine au o “slăbiciune exploatabilă” pe termen lung — nu doar în faza inițială de tratament.
Ce nu se schimbă — și ce trebuie să știi cu prudență
- Faptul că ai mutația nu garantează că toate terapiile vor funcționa — unele celule canceroase pot dezvolta mecanisme de rezistență la inhibitorii PARP în timp.
- Nu toate paciente cu mutație BRCA pot fi eligibile pentru olaparib (sau alte PARP) — trebuie să îndeplinești criterii de risc (dimensiune tumorală, ganglioni implicați etc.).
- Tratamentul personalizat necesită monitorizare atentă a efectelor secundare (de exemplu, scăderea numărului de celule sanguine) și ajustări.
- Costul, accesul la medicament și aprobările locale/rambursarea pot reprezenta obstacole (nu toate țările sau sistemele de sănătate au adoptat deja aceste terapii pentru toate cazurile eligibile).
Mesajul esențial
Aflarea mutației BRCA nu este o sentință — este o informație care poate schimba tratamentul în favoarea ta. Defectul de reparare a ADN-ului, prezent în celulele canceroase, devine o armă terapeutică atunci când știm cum să îl folosim. Genetica nu te definește, dar îi poate oferi medicului tău harta exactă a locului în care boala este vulnerabilă. Iar asta înseamnă o șansă reală în plus.
Surse și recomandări
Articolul se bazează pe ghidurile actualizate ale ASCO, ESMO și NCCN, precum și pe rezultatele studiilor clinice majore (OlympiA – olaparib adjuvant). Deciziile terapeutice se stabilesc întotdeauna individual, împreună cu echipa ta oncologică.
Conținut educațional HER Genes. Nu înlocuiește consultul medical. Deciziile se iau individual, împreună cu echipa oncologică.
Susține Proiectul Asociația Gabrielle
Fiecare donație ne ajută să oferim mai mult sprijin, resurse și conținut pentru femei ca tine.
Let’s Get Social
Pe rețelele sociale suntem aproape de tine cu sfaturi utile, informații validate și povești care inspiră.
Urmărește-ne pe: @hergenes_by_drmagdaduma